

La force de rétrécissement de toute longueur d'unité à la surface du liquide est appelée tension de surface, et l'unité est N. · M-1.

La propriété de la réduction de la tension de surface du solvant est appelée activité de surface, et une substance avec cette propriété est appelée substance active en surface.
La substance active de surface qui peut se lier des molécules dans une solution aqueuse et former des micelles et d'autres associations, et a une activité de surface élevée, tout en ayant l'effet de mouiller, d'émulsification, de moussage, de lavage, etc. est appelé surfactant.
Le tensioactif est des composés organiques avec une structure et une propriété spéciales, ce qui peut modifier considérablement la tension interfaciale entre deux phases ou la tension en surface des liquides (généralement l'eau), avec des propriétés mouillées, moussantes, émulsifiantes, lavage et autres propriétés.
En termes de structure, les tensioactifs ont une caractéristique commune en ce qu'ils contiennent deux groupes de nature différente dans leurs molécules. À une extrémité se trouve une longue chaîne de groupe non polaire, soluble dans l'huile et insoluble dans l'eau, également connue sous le nom de groupe hydrophobe ou groupe hydrofuge. Un tel groupe hydrofuge est généralement de longues chaînes d'hydrocarbures, parfois aussi pour le fluor organique, le silicium, l'organophosphate, la chaîne d'organotine, etc. À l'autre extrémité se trouve un groupe soluble dans l'eau, un groupe hydrophile ou un groupe d'huile. Le groupe hydrophile doit être suffisamment hydrophile pour garantir que les tensioactifs entiers sont solubles dans l'eau et ont la solubilité nécessaire. Étant donné que les tensioactifs contiennent des groupes hydrophiles et hydrophobes, ils peuvent être solubles dans au moins une des phases liquides. Cette propriété hydrophile et lipophile du tensioactif est appelée amphiphilicité.


Le tensioactif est une sorte de molécules amphiphiles avec des groupes hydrophobes et hydrophiles. Les groupes hydrophobes de tensioactifs sont généralement composés d'hydrocarbures à chaîne longue, tels que l'alkyl C8 ~ C20 à chaîne droite, l'alkyl C8 ~ C20 , à chaîne ramifiée (le nombre d'alkyl carbone Tom est de 8 ~ 16) et le like. La différence qui est faible entre les groupes hydrophobes est principalement dans les changements structurels des chaînes d'hydrocarbures. Et les types de groupes hydrophiles sont plus, donc les propriétés des tensioactifs sont principalement liées aux groupes hydrophiles en plus de la taille et de la forme des groupes hydrophobes. Les changements structurels des groupes hydrophiles sont plus grands que ceux des groupes hydrophobes, de sorte que la classification des tensioactifs est généralement basée sur la structure des groupes hydrophiles. Cette classification est basée sur la question de savoir si le groupe hydrophile est ionique ou non, et il est divisé en anionique, cationique, non ionique, zwitterionique et d'autres types de surfactants spéciaux.

① Adsorption des tensioactifs à l'interfac
Les molécules de surfactant sont des molécules amphiphiles ayant des groupes lipophiles et hydrophiles. Lorsque le tensioactif est dissous dans l'eau, son groupe hydrophile est attiré par l'eau et se dissout dans l'eau, tandis que son groupe lipophile est repoussé par l'eau et laisse l'eau, entraînant l'adsorption des molécules de surfactant (ou ions) sur l'interface des deux phases, ce qui réduit la tension interfaciale entre les deux phases. Plus les molécules (ou ions) plus tensioactifs sont adsorbées à l'interface, plus la réduction de la tension interfaciale est grande.
② Certaines propriétés de la membrane d'adsorption
Pression de surface de la membrane d'adsorption: adsorption du surfactant à l'interface gaz-liquide pour former une membrane d'adsorption, comme placer une feuille flottante amovible sans frottement sur l'interface, la feuille flottante pousse la membrane adsorbante le long de la surface de la solution, et la membrane génère une pression sur la feuille de flottement, qui est appelée pression de surface.
Viscosité de surface: Comme la pression de surface, la viscosité de surface est une propriété présentée par une membrane moléculaire insoluble. Suspendu par un anneau de platine en fil métallique fin, de sorte que son plan entre en contact avec la surface de l'eau du réservoir tourne le cycle en platine, l'anneau de platine par la viscosité de l'obstacle à l'eau, l'amplitude se décompose progressivement, selon laquelle la viscosité de surface peut être mesurée. La méthode est: Premièrement, l'expérience est menée sur la surface de l'eau pure pour mesurer la décroissance de l'amplitude, puis la décroissance après la formation de la membrane de surface est mesurée, et la viscosité de la membrane de surface est dérivée de la différence entre les deux.
La viscosité de surface est étroitement liée à la solidité de la membrane de surface, et comme la membrane d'adsorption a une pression de surface et une viscosité, elle doit avoir l'élasticité. Plus la pression de surface est élevée et plus la viscosité de la membrane adsorbée est élevée, plus son module élastique est élevé. Le module élastique de la membrane d'adsorption de surface est important dans le processus de stabilisation des bulles.
③ Formation de micelles
Les solutions diluées de surfactants obéissent aux lois suivies par des solutions idéales. La quantité de tensioactif adsorbé à la surface de la solution augmente avec la concentration de la solution, et lorsque la concentration atteint ou dépasse une certaine valeur, la quantité d'adsorption n'augmente plus, et ces molécules de surfactant en excès sont dans la solution de manière au hasard ou d'une manière régulière. La pratique et la théorie montrent qu'elles forment des associations en solution, et ces associations sont appelées micelles.
Concentration critique de micelles (CMC): La concentration minimale à laquelle les tensioactifs forment des micelles en solution sont appelés concentration critique de micelle.
④ Valeurs CMC des tensioactifs communs.

Le HLB est l'abréviation de l'équilibre des lipophiles hydrophiles, qui indique l'équilibre hydrophile et lipophile des groupes hydrophiles et lipophiles du surfactant, c'est-à-dire la valeur HLB du surfactant. Une grande valeur HLB indique une molécule avec une forte hydrophilie et une faible lipophilicité; Inversement, une lipophilicité forte et une faible hydrophilie.
① Dispositions de la valeur HLB
La valeur HLB est une valeur relative, donc lorsque la valeur HLB est développée, en standard, la valeur HLB de la paraffine de cire, qui n'a pas de propriétés hydrophiliques, est spécifiée pour être 0, tandis que la valeur HLB du dodécyl sulfate de sodium, qui est plus soluble dans l'eau, est de 40. sont lipophiles, tandis que ceux supérieurs à 10 sont hydrophiles. Ainsi, le tournant du lipophile à l'hydrophile est d'environ 10.
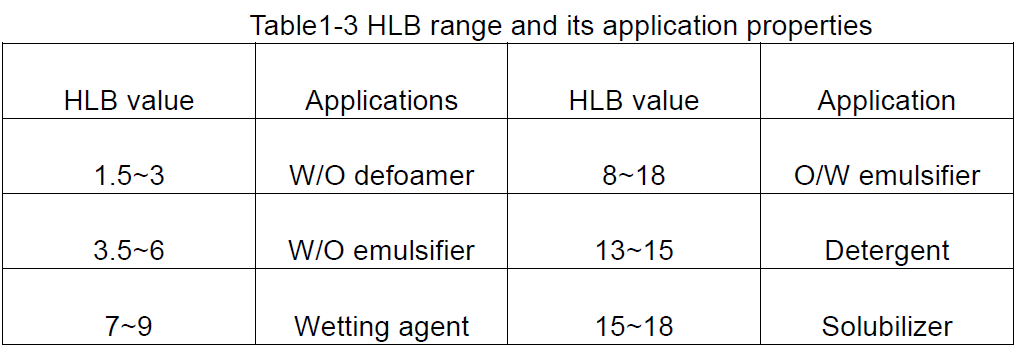
Sur la base des valeurs HLB des tensioactifs, une idée générale de leurs utilisations possibles peut être obtenue, comme le montre le tableau 1-3.

Deux liquides mutuellement insolubles, l'un dispersé dans l'autre comme des particules (gouttelettes ou cristaux liquides) forment un système appelé émulsion. Ce système est thermodynamiquement instable en raison de l'augmentation de la zone limite des deux liquides lorsque l'émulsion est formée. Afin de rendre l'émulsion stable, il est nécessaire d'ajouter un troisième composant - émulsifiant pour réduire l'énergie interfaciale du système. L'émulsifiant appartient au tensioactif, sa fonction principale est de jouer le rôle de l'émulsion. La phase de l'émulsion qui existe en tant que gouttelettes est appelée phase dispersée (ou phase intérieure, phase discontinue), et l'autre phase liée ensemble est appelée milieu de dispersion (ou phase extérieure, phase continue).
① Emulsifiants et émulsions
Émulsions communes, une phase est l'eau ou la solution aqueuse, l'autre phase est des substances organiques non miscibles avec de l'eau, telles que la graisse, la cire, etc. L'émulsion formée en eau et en huile peut être divisée en deux types en fonction de leur situation de dispersion: l'huile dispersée dans l'eau pour former de l'huile dans un type émulsion, exprimée en tant qu'O / W (eau): Water dispersé en pétrole pour former l'huile-in-water Tyle EMULLION, exprimé): Water Disted in Oil to Oil In-in-water Tyle Type, a exprimé: O-WA (Eau / huile). Eau complexe dans l'huile dans l'eau avec type O / W et huile dans l'eau dans l'huile O / O / S multi-émulsions peuvent également être formées.
Les émulsifiants sont utilisés pour stabiliser les émulsions en réduisant la tension interfaciale et en formant une membrane interfaciale à molécule unique.
Dans l'émulsification des exigences de l'émulsifiant:
R: L'émulsifiant doit être capable d'adsorber ou d'enrichir l'interface entre les deux phases, de sorte que la tension interfaciale est réduite;
B: L'émulsifiant doit donner les particules à la charge, de sorte que la répulsion électrostatique entre les particules, ou forme une membrane protectrice stable et très visqueuse autour des particules.
Par conséquent, la substance utilisée comme émulsifiant doit avoir des groupes amphiphiles pour émulsifier, et les tensioactifs peuvent répondre à cette exigence.
② Méthodes de préparation des émulsions et des facteurs affectant la stabilité des émulsions
Il existe deux façons de préparer les émulsions: la première consiste à utiliser la méthode mécanique pour disperser le liquide dans de minuscules particules dans un autre liquide, qui est principalement utilisé dans l'industrie pour préparer des émulsions; L'autre consiste à dissoudre le liquide à l'état moléculaire dans un autre liquide, puis à le rassembler correctement pour former des émulsions.
La stabilité d'une émulsion est la capacité d'agrégation anti-particules qui conduit à la séparation des phases. Les émulsions sont des systèmes thermodynamiquement instables avec une grande énergie libre. Par conséquent, la soi-disant stabilité d'une émulsion est en fait le temps nécessaire pour que le système atteigne l'équilibre, c'est-à-dire le temps nécessaire pour la séparation de l'un des liquides du système.
Lorsque la membrane interfaciale avec des alcools gras, des acides gras et des amines gras et d'autres molécules organiques polaires, la résistance à la membrane est significativement plus élevée. En effet, dans la couche d'adsorption interfaciale des molécules et alcools d'émulsification, des acides et des amines et d'autres molécules polaires pour former un "complexe", de sorte que la résistance à la membrane interfaciale a augmenté.
Les émulsifiants constitués de plus de deux tensioactifs sont appelés émulsifiants mixtes. Émulsifiant mixte adsorbé à l'interface eau / huile; L'action intermoléculaire peut former des complexes. En raison de la forte action intermoléculaire, la tension interfaciale est considérablement réduite, la quantité d'émulsifiant adsorbé à l'interface est considérablement augmentée, la formation de densité de membrane interfaciale augmente, la résistance augmente.
La charge des billes liquides a un effet significatif sur la stabilité de l'émulsion. Émulsions stables, dont les perles liquides sont généralement chargées. Lorsqu'un émulsifiant ionique est utilisé, l'émulsifiant adsorbé à l'interface a son groupe lipophile inséré dans la phase huileuse et le groupe hydrophile est en phase hydrique, ce qui rend les billes liquides chargées. Comme les perles d'émulsion avec la même charge, ils se repoussent, pas faciles à agglomérer, de sorte que la stabilité est augmentée. On peut voir que plus les ions émulsifiants adsorbés sur les billes, plus la charge est grande, plus la capacité d'empêcher les perles d'agglomération soit grande, plus le système d'émulsion est stable.
La viscosité du milieu de dispersion de l'émulsion a une certaine influence sur la stabilité de l'émulsion. Généralement, plus la viscosité du milieu de dispersion est élevée, plus la stabilité de l'émulsion est élevée. En effet, la viscosité du milieu de dispersion est grande, ce qui a un effet fort sur le mouvement brownien des billes liquides et ralentit la collision entre les billes liquides, de sorte que le système reste stable. Habituellement, les substances polymères qui peuvent être dissoutes dans les émulsions peuvent augmenter la viscosité du système et augmenter la stabilité des émulsions. De plus, les polymères peuvent également former une forte membrane interfaciale, ce qui rend le système d'émulsion plus stable.
Dans certains cas, l'ajout de poudre solide peut également faire en sorte que l'émulsion a tendance à se stabiliser. La poudre solide est dans l'eau, l'huile ou l'interface, selon l'huile, l'eau sur la capacité de mouillage de la poudre solide, si la poudre solide n'est pas complètement mouillée avec de l'eau, mais également humide par l'huile, restera sur l'interface de l'eau et de l'huile.
La poudre solide ne rend pas l'émulsion stable car la poudre recueillie à l'interface améliore la membrane interfaciale, qui est similaire à l'adsorption interfaciale des molécules d'émulsifiant, donc plus le matériau de poudre solide est disposé à l'interface, plus l'émulsion est stable.
Les tensioactifs ont la capacité d'augmenter considérablement la solubilité des substances organiques insolubles ou légèrement solubles dans l'eau après avoir formé des micelles en solution aqueuse, et la solution est transparente à l'heure actuelle. Cet effet de la micelle est appelé solubilisation. Le tensioactif qui peut produire de la solubilisation est appelé solubilisation, et la matière organique qui est solubilisée est appelée matière solubilisée.

La mousse joue un rôle important dans le processus de lavage. La mousse est un système de dispersion dans lequel un gaz est dispersé dans un liquide ou solide, avec le gaz comme phase dispersée et le liquide ou solide comme milieu de dispersion, le premier étant appelé mousse liquide, tandis que le second est appelé mousse solide, comme le plastique moussé, le verre moussé, le ciment moussé, etc.
(1) Formation de mousse
Par mousse, nous entendons ici un agrégat de bulles d'air séparées par une membrane liquide. Ce type de bulle monte toujours rapidement à la surface du liquide en raison de la grande différence de densité entre la phase dispersée (gaz) et le milieu de dispersion (liquide), combinée à la faible viscosité du liquide.
Le processus de formation d'une bulle consiste à apporter une grande quantité de gaz dans le liquide, et les bulles du liquide reviennent rapidement à la surface, formant un agrégat de bulles séparées par une petite quantité de gaz liquide.
La mousse a deux caractéristiques significatives en termes de morphologie: l'une est que les bulles en tant que phase dispersée sont souvent de forme polyédrique, c'est parce qu'à l'intersection des bulles, il y a une tendance à la fin du film liquide pour que les bulles deviennent polyédriques, lorsque le film liquide se termine à une certaine étendue, il mène à la rupture de bulles; La seconde est que les liquides purs ne peuvent pas former de la mousse stable, le liquide qui peut former de la mousse est d'au moins deux composants ou plus. Les solutions aqueuses de surfactants sont typiques des systèmes sujets à la génération de mousse, et leur capacité à générer de la mousse est également liée à d'autres propriétés.
Les tensioactifs avec une bonne puissance moussante sont appelés agents moussants. Bien que l'agent moussant ait une bonne capacité en mousse, mais la mousse formée peut ne pas être en mesure de maintenir longtemps, c'est-à-dire que sa stabilité n'est pas nécessairement bonne. Afin de maintenir la stabilité de la mousse, souvent dans l'agent moussant pour ajouter des substances qui peuvent augmenter la stabilité de la mousse, la substance est appelée stabilisateur de mousse, le stabilisateur couramment utilisé est le lauryl diéthanolamine et l'oxyde de dodécyl diméthylamine.
(2) stabilité de la mousse
La mousse est un système thermodynamiquement instable et la tendance finale est que la surface totale du liquide dans le système diminue après la baisse de la bulle et que l'énergie libre diminue. Le processus de défilage est le processus par lequel la membrane liquide séparant le gaz devient plus épais et plus mince jusqu'à ce qu'elle se casse. Par conséquent, le degré de stabilité de la mousse est principalement déterminé par la vitesse de décharge liquide et la résistance du film liquide. Les facteurs suivants influencent également cela.
(3) Destruction de la mousse
Le principe de base de la destruction de la mousse est de modifier les conditions qui produisent la mousse ou d'éliminer les facteurs de stabilisation de la mousse, il existe donc des méthodes physiques et chimiques de désabonnement.
Le dédouage physique signifie modifier les conditions de production de mousse tout en maintenant la composition chimique de la solution de mousse, telles que les perturbations externes, les changements de température ou de pression et le traitement ultrasonique sont toutes des méthodes physiques efficaces pour éliminer la mousse.
La méthode de dédouage chimique consiste à ajouter certaines substances pour interagir avec l'agent moussant pour réduire la résistance du film liquide dans la mousse et ainsi réduire la stabilité de la mousse pour atteindre l'objectif de dédouage, ces substances sont appelées DefoAmères. La plupart des défoamères sont des surfactants. Par conséquent, selon le mécanisme de défilage, le défoamère devrait avoir une forte capacité à réduire la tension de surface, facile à adsorber à la surface et l'interaction entre les molécules d'adsorption de surface est faible, les molécules d'adsorption disposées dans une structure plus desserrée.
Il existe différents types de défoamère, mais en gros, ce sont tous des tensioactifs non ioniques. Les tensioactifs non ioniques ont des propriétés anti-monnaie à proximité ou au-dessus de leur point de nuage et sont souvent utilisées comme défoamères. Les alcools, en particulier les alcools avec une structure de ramification, les acides gras et les esters d'acide gras, les polyamides, les esters de phosphate, les huiles de silicone, etc. sont également couramment utilisés comme excellents dédomultes.
(4) mousse et lavage
Il n'y a pas de lien direct entre la mousse et l'efficacité du lavage et la quantité de mousse n'indique pas l'efficacité du lavage. Par exemple, les tensioactifs non ioniques ont beaucoup moins de propriétés moussantes que les savons, mais leur décontamination est bien meilleure que les savons.
Dans certains cas, la mousse peut être utile pour éliminer la saleté et la crasse. Par exemple, lors du lavage de la vaisselle à la maison, la mousse du détergent ramasse les gouttelettes d'huile et lors du frottement des tapis, la mousse aide à ramasser la poussière, la poudre et d'autres saletés solides. De plus, la mousse peut parfois être utilisée comme indication de l'efficacité d'un détergent. Parce que les huiles grasses ont un effet inhibant sur la mousse du détergent, lorsqu'il y a trop d'huile et trop peu de détergent, aucune mousse ne sera générée ou que la mousse d'origine disparaîtra. La mousse peut également parfois être utilisée comme indicateur de la propreté d'un rinçage, car la quantité de mousse dans la solution de rinçage a tendance à diminuer avec la réduction du détergent, de sorte que la quantité de mousse peut être utilisée pour évaluer le degré de rinçage.
Dans un sens large, le lavage est le processus d'élimination des composants indésirables de l'objet à laver et d'atteindre un objectif. Le lavage dans le sens habituel fait référence au processus d'élimination de la saleté de la surface du transporteur. Dans le lavage, l'interaction entre la saleté et le support est affaiblie ou éliminée par l'action de certaines substances chimiques (par exemple, détergent, etc.), de sorte que la combinaison de la saleté et du support est changée en combinaison de saleté et de détergent, et enfin la saleté est séparée du support. Comme les objets à laver et que la saleté à éliminer est diversifiée, le lavage est un processus très complexe et le processus de base de lavage peut être exprimé dans les relations simples suivantes.
Carrie ·· Dirt + détergent = porteuse + saleté · détergent
Le processus de lavage peut généralement être divisé en deux étapes: premièrement, sous l'action du détergent, la saleté est séparée de son porte-avions; Deuxièmement, la saleté détachée est dispersée et suspendue dans le milieu. Le processus de lavage est un processus réversible et la saleté dispersée et suspendue dans le milieu peut également être re-precipitée du milieu à l'objet lavé. Par conséquent, un bon détergent devrait avoir la capacité de disperser et de suspendre la saleté et d'empêcher la redéposition de la saleté, en plus de la capacité d'éliminer la saleté du support.
(1) Types de saleté
Même pour le même élément, le type, la composition et la quantité de saleté peuvent varier en fonction de l'environnement dans lequel il est utilisé. La saleté du corps de l'huile est principalement certaines huiles animales et végétales et huiles minérales (comme l'huile brute, le pétrole, le goudron de charbon, etc.), la saleté solide est principalement de la suie, de la cendre, de la rouille, du noir de carbone, etc. En termes de saleté de vêtements, il y a de la saleté du corps humain, comme la transpiration, le sébum, le sang, etc.; Dirt des aliments, tels que les taches de fruits, les taches d'huile de cuisson, les taches de condiments, l'amidon, etc.; Dirt des cosmétiques, comme le rouge à lèvres, le vernis à ongles, etc.; Dirt de l'atmosphère, comme la suie, la poussière, la boue, etc.; D'autres, comme l'encre, le thé, le revêtement, etc. Il est disponible en différents types.
Les différents types de saleté peuvent généralement être divisés en trois catégories principales: la saleté solide, la saleté liquide et la saleté spéciale.
① Dirt solide
La saleté solide commune comprend des particules de cendres, de la boue, de la terre, de la rouille et du noir de carbone. La plupart de ces particules ont une charge électrique à leur surface, la plupart d'entre elles sont chargées négativement et peuvent être facilement adsorbées sur des éléments de fibres. La saleté solide est généralement difficile à dissoudre dans l'eau, mais peut être dispersée et suspendue par des solutions détergentes. La saleté solide avec un point de masse plus petit est plus difficile à éliminer.
② Dirt liquide
La saleté liquide est principalement soluble à l'huile, y compris les huiles végétales et animales, les acides gras, les alcools gras, les huiles minérales et leurs oxydes. Parmi eux, les huiles végétales et animales, les acides gras et la saponification des alcalins peuvent se produire, tandis que les alcools gras, les huiles minérales ne sont pas saponifiés par les alcalins, mais peuvent être solubles dans les alcools, les éthers et les solvants organiques hydrocarbonés et la solution d'eau détergente émulsification et dispersion. La saleté liquide soluble à l'huile a généralement une force forte avec des articles en fibres et est plus fermement adsorbé sur les fibres.
③ Dirt spécial
La saleté spéciale comprend les protéines, l'amidon, le sang, les sécrétions humaines telles que la transpiration, le sébum, le jus d'urine et de fruits et le jus de thé. La majeure partie de ce type de saleté peut être chimiquement et fortement adsorbée sur des articles en fibre. Par conséquent, il est difficile de se laver.
Les différents types de saleté sont rarement trouvés seuls, mais sont souvent mélangés et adsorbés sur l'objet. La saleté peut parfois être oxydée, décomposée ou décomposée sous des influences externes, créant ainsi une nouvelle saleté.
(2) Adhésion de la saleté
Les vêtements, les mains, etc. peuvent être tachés car il existe une sorte d'interaction entre l'objet et la saleté. La saleté adhère aux objets de diverses manières, mais il n'y a rien de plus que des adhérences physiques et chimiques.
① L'adhésion de la suie, de la poussière, de la boue, du sable et du charbon de bois aux vêtements est une adhérence physique. De manière générale, grâce à cette adhérence de la saleté, et le rôle entre l'objet coloré est relativement faible, l'élimination de la saleté est également relativement facile. Selon les différentes forces, l'adhésion physique de la saleté peut être divisée en adhésion mécanique et adhésion électrostatique.
R: Adhésion mécanique
Ce type d'adhésion se réfère principalement à l'adhésion d'une saleté solide (par exemple, de la poussière, de la boue et du sable). L'adhésion mécanique est l'une des formes les plus faibles d'adhésion de la saleté et peut être éliminée presque par des moyens purement mécaniques, mais lorsque la saleté est petite (<0,1), il est plus difficile à éliminer.
B : Adhésion électrostatique
L'adhésion électrostatique se manifeste principalement dans l'action des particules de saleté chargées sur des objets chargés de charge opposée. La plupart des objets fibreux sont chargés négativement dans l'eau et peuvent facilement être respectés par certaines saletés chargées positivement, comme les types de chaux. Une certaine saleté, bien que négativement chargée, comme les particules de noir de carbone dans des solutions aqueuses, peut adhérer aux fibres à travers des ponts ioniques (ions entre plusieurs objets à charge opposée, agissant avec eux d'une manière semblable à un pont) formé par des ions positifs dans l'eau (par exemple, Ca2 + , Mg2 + etc.).
L'action électrostatique est plus forte que la simple action mécanique, ce qui rend la suppression de la saleté relativement difficile.
② Adhésion chimique
L'adhésion chimique fait référence au phénomène de la saleté agissant sur un objet par des liaisons chimiques ou hydrogène. Par exemple, la saleté solide polaire, les protéines, la rouille et d'autres adhésions sur les articles en fibres, les fibres contiennent des groupes carboxyle, hydroxyle, amide et autres groupes, ces groupes et les acides gras de saleté grasse, les alcools gras sont faciles à former des liaisons hydrogène. Les forces chimiques sont généralement fortes et la saleté est donc plus fermement liée à l'objet. Ce type de saleté est difficile à éliminer par les méthodes habituelles et nécessite des méthodes spéciales pour y faire face.
Le degré d'adhésion de la saleté est lié à la nature de la saleté elle-même et à la nature de l'objet auquel il est adhéré. Généralement, les particules adhèrent facilement aux éléments fibreux. Plus la texture de la saleté solide est petite, plus l'adhésion est forte. La saleté polaire sur des objets hydrophiles tels que le coton et le verre adhèrent plus fortement que la saleté non polaire. La saleté non polaire adhère plus fortement que la saleté polaire, comme les graisses polaires, la poussière et l'argile, et est moins facile à éliminer et à nettoyer.
(3) Mécanisme d'élimination de la saleté
Le but du lavage est d'éliminer la saleté. Dans un moyen d'une certaine température (principalement de l'eau). En utilisant les divers effets physiques et chimiques du détergent pour affaiblir ou éliminer l'effet de la saleté et des objets lavés, sous l'action de certaines forces mécaniques (comme le frottement à la main, l'agitation de la machine à laver, l'impact de l'eau), de sorte que la saleté et les objets lavés du but de la décontamination.
① Mécanisme de l'élimination de la saleté liquide
A : mouillage
Les salissures liquides sont principalement à base d'huile. Les taches d'huile mouillent la plupart des articles fibreux et se propagent plus ou moins en tant que film d'huile à la surface du matériau fibreux. La première étape de l'action de lavage est le mouillage de la surface par le liquide de lavage. Par souci d'illustration, la surface d'une fibre peut être considérée comme une surface solide lisse.
B: Détachement de l'huile - Mécanisme de curling
La deuxième étape de l'action de lavage est l'élimination de l'huile et de la graisse, l'élimination de la saleté liquide est obtenue par une sorte de bobinage. La saleté liquide existait à l'origine à la surface sous la forme d'un film d'huile étalé, et sous l'effet de mouillage préférentiel du liquide de lavage sur la surface solide (c'est-à-dire la surface de la fibre), il s'est recroquevillé dans des perles d'huile étape par étape, qui ont été remplacées par le liquide de lavage et ont finalement quitté la surface sous certaines forces externes.
② Mécanisme de l'élimination solide de la saleté
L'élimination de la saleté liquide se fait principalement par le mouillage préférentiel de la porteuse de saleté par la solution de lavage, tandis que le mécanisme d'élimination de la saleté solide est différent, où le processus de lavage concerne principalement le mouillage de la masse de la saleté et de la surface de sa porteuse par la solution de lavage. En raison de l'adsorption des tensioactifs sur la saleté solide et la surface de sa porteuse, l'interaction entre la saleté et la surface est réduite et la résistance à l'adhésion de la masse de la saleté sur la surface est réduite, donc la masse de la saleté est facilement retirée de la surface de la porteuse.
De plus, l'adsorption des tensioactifs, en particulier des tensioactifs ioniques, à la surface de la saleté solide et de son support a le potentiel d'augmenter le potentiel de surface à la surface de la saleté solide et de son support, ce qui est plus propice à l'élimination de la saleté. Les surfaces solides ou généralement fibreuses sont généralement chargées négativement dans des milieux aqueuses et peuvent donc former des couches diffuses à double électronique sur des masses de saleté ou des surfaces solides. En raison de la répulsion des charges homogènes, l'adhésion des particules de saleté dans l'eau à la surface solide est affaiblie. Lorsqu'un tensioactif anionique est ajouté, car il peut simultanément augmenter le potentiel de surface négatif de la particule de saleté et de la surface solide, la répulsion entre elles est plus améliorée, la résistance à l'adhésion de la particule est plus réduite et la saleté est plus facile à éliminer.
Les tensioactifs non ioniques sont adsorbés sur des surfaces solides généralement chargées et bien qu'elles ne changent pas de manière significative le potentiel interfacial, les surfactants non ioniques adsorbés ont tendance à former une certaine épaisseur de couche adsorbée à la surface qui aide à prévenir le redéposition de la saleté.
Dans le cas des tensioactifs cationiques, leur adsorption réduit ou élimine le potentiel de surface négatif de la masse de la saleté et de sa surface porteuse, ce qui réduit la répulsion entre la saleté et la surface et n'est donc pas propice à l'élimination de la saleté; De plus, après adsorption sur la surface solide, les tensioactifs cationiques ont tendance à tourner la surface solide hydrophobe et ne sont donc pas propices au mouillage de surface et donc au lavage.
③ Élimination des sols spéciaux
Les protéines, l'amidon, les sécrétions humaines, le jus de fruits, le jus de thé et d'autres sales sont difficiles à éliminer avec des tensioactifs normaux et nécessitent un traitement spécial.
Les taches de protéines telles que la crème, les œufs, le sang, le lait et les excréments cutanés ont tendance à coaguler sur les fibres et la dégénérescence et à obtenir une adhésion plus forte. Les salissures en protéines peuvent être éliminées en utilisant des protéases. L'enzyme protéase décompose les protéines de la saleté en acides aminés solubles dans l'eau ou oligopeptides.
Les taches d'amidon proviennent principalement de denrées alimentaires, d'autres telles que la sauce, la colle, etc. L'amylase a un effet catalytique sur l'hydrolyse des taches d'amidon, provoquant la décomposition de l'amidon en sucres.
La lipase catalyse la décomposition de triglycérides, qui sont difficiles à éliminer par des méthodes normales, telles que le sébum et les huiles comestibles, et les décompose en glycérol soluble et acides gras.
Certaines taches colorées des jus de fruits, des jus de thé, des encres, du rouge à lèvres, etc. sont souvent difficiles à nettoyer soigneusement même après un lavage répété. Ces taches peuvent être éliminées par une réaction redox avec un agent oxydant ou réducteur tel que Javel, qui détruit la structure des groupes générateurs de couleurs ou de couleurs et les dégrade en composants solubles plus petits.
(4) Mécanisme d'élimination des taches du nettoyage à sec
Ce qui précède est en fait pour l'eau comme moyen de laver. En fait, en raison des différents types de vêtements et de structure, certains vêtements utilisant le lavage de l'eau ne sont pas pratiques ou pas faciles à nettoyer, certains vêtements après lavage et même déformation, décoloration, etc., par exemple: la plupart des fibres naturelles absorbent l'eau et facile à gonfler, et à sec et facile à réduire, donc après le lavage sera déformé; En lavant les produits en laine semblent également souvent un phénomène de retrait, certains produits en laine avec lavage d'eau sont également faciles à piller, le changement de couleur; Certaines sensations de soie deviennent pires après le lavage et perdent leur éclat. Pour ces vêtements, utilisez souvent la méthode de nettoyage à sec pour décontaminer. Le soi-disant nettoyage à sec fait généralement référence à la méthode de lavage dans les solvants organiques, en particulier dans les solvants non polaires.
Le nettoyage à sec est une forme plus douce de lavage que le lavage de l'eau. Parce que le nettoyage à sec ne nécessite pas beaucoup d'action mécanique, il ne cause pas de dommages, de rides et de déformation aux vêtements, tandis que les agents de nettoyage à sec, contrairement à l'eau, produisent rarement l'expansion et la contraction. Tant que la technologie est correctement gérée, les vêtements peuvent être nettoyés à sec sans distorsion, décoloration des couleurs et durée de vie prolongée.
En termes de nettoyage à sec, il existe trois grands types de saleté.
La saleté soluble sur l'huile soluble, la saleté comprend toutes sortes d'huile et de graisse, qui est liquide ou grasse et peut être dissoute dans des solvants de nettoyage à sec.
La saleté soluble dans l'eau soluble dans l'eau est soluble dans des solutions aqueuses, mais pas dans les agents de nettoyage à sec, est adsorbé sur les vêtements à l'état aqueux, l'eau s'évapore après la précipitation de solides granulaires, comme les sels inorganiques, l'amidon, les protéines, etc.
③oile et eau Insoluble L'huile de saleté et la saleté insoluble dans l'eau n'est ni soluble dans l'eau ni soluble dans les solvants de nettoyage à sec, comme le noir de carbone, les silicates de divers métaux et oxydes, etc.
En raison de la nature différente de divers types de saleté, il existe différentes façons d'éliminer la saleté dans le processus de nettoyage à sec. Les sols solubles à l'huile, tels que les huiles animales et végétaux, les huiles minérales et les graisses, sont facilement solubles dans les solvants organiques et peuvent être éliminés plus facilement dans le nettoyage à sec. L'excellente solubilité des solvants de nettoyage à sec pour les huiles et les graisses provient essentiellement des forces des murs de van der entre les molécules.
Pour l'élimination de la saleté soluble dans l'eau, comme les sels inorganiques, les sucres, les protéines et la transpiration, la bonne quantité d'eau doit également être ajoutée à l'agent de nettoyage à sec, sinon la saleté soluble dans l'eau est difficile à éliminer des vêtements. Cependant, l'eau est difficile à dissoudre dans l'agent de nettoyage à sec, donc pour augmenter la quantité d'eau, vous devez également ajouter des tensioactifs. La présence d'eau dans l'agent de nettoyage à sec peut rendre la surface de la saleté et des vêtements hydratés, de sorte qu'il est facile d'interagir avec les groupes polaires de surfactants, ce qui est propice à l'adsorption des tensioactifs à la surface. De plus, lorsque les tensioactifs forment des micelles, la saleté et l'eau solubles dans l'eau peuvent être solubilisées dans les micelles. En plus d'augmenter la teneur en eau du solvant de nettoyage à sec, les tensioactifs peuvent également jouer un rôle dans la prévention de la redéposition de la saleté pour améliorer l'effet de décontamination.
La présence d'une petite quantité d'eau est nécessaire pour éliminer la saleté soluble dans l'eau, mais trop d'eau peut provoquer une distorsion et des rides dans certains vêtements, de sorte que la quantité d'eau dans l'agent de nettoyage à sec doit être modérée.
La saleté qui n'est ni soluble dans l'eau ni soluble à l'huile, des particules solides comme les cendres, la boue, la terre et le noir de carbone, est généralement attachée au vêtement par des forces électrostatiques ou en combinaison avec de l'huile. Dans le nettoyage à sec, le flux de solvant, l'impact peut rendre l'adsorption de la force électrostatique de la saleté, et l'agent de nettoyage à sec peut dissoudre l'huile, de sorte que la combinaison d'huile et de saleté et attachée aux vêtements de particules solides dans l'agent de nettoyage à sec, l'agent de nettoyage à sec dans une petite quantité d'eau et les surfacants, afin que les particules de la saleté puissantes puissent être une disposition.
(5) Facteurs affectant l'action de lavage
L'adsorption directionnelle des tensioactifs à l'interface et la réduction de la tension de surface (interfaciale) sont les principaux facteurs de l'élimination de la saleté liquide ou solide. Cependant, le processus de lavage est complexe et l'effet de lavage, même avec le même type de détergent, est influencé par de nombreux autres facteurs. Ces facteurs incluent la concentration du détergent, la température, la nature des salissages, le type de fibre et la structure du tissu.
① Concentration de surfactant
Les micelles de tensioactifs en solution jouent un rôle important dans le processus de lavage. Lorsque la concentration atteint la concentration critique de micelle (CMC), l'effet de lavage augmente fortement. Par conséquent, la concentration de détergent dans le solvant doit être supérieure à la valeur CMC pour avoir un bon effet de lavage. Cependant, lorsque la concentration de tensioactif est supérieure à la valeur CMC, l'augmentation incrémentielle de l'effet de lavage n'est pas évidente et il n'est pas nécessaire d'augmenter trop la concentration de surfactant.
Lors de l'élimination de l'huile par solubilisation, l'effet de solubilisation augmente avec l'augmentation de la concentration de surfactant, même lorsque la concentration est supérieure à la CMC. À l'heure actuelle, il est conseillé d'utiliser un détergent de manière centralisée locale. Par exemple, s'il y a beaucoup de saleté sur les poignets et le col d'un vêtement, une couche de détergent peut être appliquée pendant le lavage pour augmenter l'effet de solubilisation du surfactant sur l'huile.
La température a une influence très importante sur l'action de décontamination. En général, l'augmentation de la température facilite l'élimination de la saleté, mais parfois une température trop élevée peut également provoquer des inconvénients.
L'augmentation de la température facilite la diffusion de la saleté, la graisse solide est facilement émulsifiée à des températures supérieures à son point de fusion et l'augmentation des fibres de gonflement en raison de l'augmentation de la température, qui facilitent toutes l'élimination de la saleté. Cependant, pour les tissus compacts, les microgaps entre les fibres sont réduits à mesure que les fibres se développent, ce qui est préjudiciable à l'élimination de la saleté.
Les changements de température affectent également la solubilité, la valeur CMC et la taille des micelles des tensioactifs, affectant ainsi l'effet de lavage. La solubilité des tensioactifs avec de longues chaînes de carbone est faible à basse température et parfois la solubilité est encore plus faible que la valeur CMC, de sorte que la température de lavage doit être augmentée de manière appropriée. L'effet de la température sur la valeur CMC et la taille des micelles est différent pour les tensioactifs ioniques et non ioniques. Pour les tensioactifs ioniques, une augmentation de la température augmente généralement la valeur CMC et réduit la taille des micelles, ce qui signifie que la concentration de tensioactif dans la solution de lavage doit être augmentée. Pour les tensioactifs non ioniques, une augmentation de la température entraîne une diminution de la valeur CMC et une augmentation significative du volume des micelles, il est donc clair qu'une augmentation appropriée de la température aidera le surfactant non ionique à exercer son effet de surface. Cependant, la température ne doit pas dépasser son point de nuage.
En bref, la température optimale de lavage dépend de la formulation du détergent et de l'objet lavé. Certains détergents ont un bon effet détergent à température ambiante, tandis que d'autres ont une détergence très différente entre le lavage froid et chaud.
③ mousse
Il est habituel de confondre le pouvoir de moussage avec l'effet de lavage, estimant que les détergents avec une puissance moussante élevée ont un bon effet de lavage. La recherche a montré qu'il n'y a pas de relation directe entre l'effet de lavage et la quantité de mousse. Par exemple, le lavage avec des détergents moussants faibles n'est pas moins efficace que le lavage avec des détergents moussants élevés.
Bien que la mousse ne soit pas directement liée au lavage, il y a des occasions où il aide à éliminer la saleté, par exemple, lors du lavage de la vaisselle à la main. Lors du frottement des tapis, la mousse peut également emporter la poussière et d'autres particules de saleté solide, la saleté du tapis représente une grande proportion de poussière, de sorte que les agents de nettoyage des tapis devraient avoir une certaine capacité de mousse.
La puissance de mousse est également importante pour les shampooings, où la mousse fine produite par le liquide pendant le shampooing ou le bain laisse les cheveux lubrifiés et confortables.
④ Variétés de fibres et de propriétés physiques des textiles
En plus de la structure chimique des fibres, qui affecte l'adhésion et l'élimination de la saleté, l'apparition des fibres et l'organisation du fil et du tissu ont une influence sur la facilité d'élimination de la saleté.
Les écailles de fibres de laine et les rubans plats incurvés de fibres de coton sont plus susceptibles d'accumuler de la saleté que les fibres lisses. Par exemple, le noir coloré en noir sur des films de cellulose (films visqueux) est facile à éliminer, tandis que le noir taché en noir sur des tissus de coton est difficile à laver. Un autre exemple est que les tissus à fibres courtes en polyester sont plus enclins à accumuler des taches d'huile que les tissus à fibres longues, et les taches d'huile sur les tissus à fibres courtes sont également plus difficiles à éliminer que les taches d'huile sur des tissus à fibres longues.
Les fils serrés et les tissus serrés, en raison du petit écart entre les fibres, peuvent résister à l'invasion de la saleté, mais il en va de même pour empêcher le liquide de lavage d'exclure la saleté interne, les tissus serrés commencent à résister à la saleté, mais une fois que le lavage tachée est également plus difficile.
⑤ dureté de l'eau
La concentration d'ions Ca2 +, Mg2 + et d'autres ions métalliques dans l'eau a une grande influence sur l'effet de lavage, en particulier lorsque les surfactants anioniques rencontrent des ions Ca2 + et Mg2 + formant des sels de calcium et de magnésium qui sont moins solubles et réduiront sa détermination. Dans l'eau dure, même si la concentration de tensioactif est élevée, la détergence est encore bien pire que dans la distillation. Pour que le tensioactif ait le meilleur effet de lavage, la concentration d'ions Ca2 + dans l'eau doit être réduite à 1 x 10-6 mol / L (CACO3 à 0,1 mg / L) ou moins. Cela nécessite l'ajout de divers adoucisseurs au détergent.
Heure du poste: février-25-2022



